Ion berikut mengalami hidrolisis dalam air kecuali: Pertanyaan ini mengantar kita ke dunia menarik reaksi kimia di dalam air. Hidrolisis, reaksi ion dengan air, menentukan sifat asam atau basa suatu larutan. Memahami proses ini krusial dalam berbagai bidang, dari kimia analitik hingga biologi. Mari kita telusuri lebih dalam tentang ion-ion yang bereaksi dan yang tidak bereaksi dengan air.
Proses hidrolisis ion melibatkan interaksi antara ion dengan molekul air, menghasilkan perubahan pH larutan. Beberapa ion, seperti anion basa konjugat dari asam lemah, akan bereaksi dengan air membentuk ion hidroksida (OH-), membuat larutan menjadi basa. Sebaliknya, kation asam konjugat dari basa lemah akan bereaksi dengan air membentuk ion hidronium (H3O+), membuat larutan menjadi asam. Namun, ada juga ion-ion yang tidak mengalami hidrolisis karena sifatnya yang netral atau karena kekuatan asam/basa konjugatnya yang sangat lemah.
Hidrolisis Ion dalam Air
Hidrolisis ion merupakan reaksi kimia yang terjadi ketika ion-ion tertentu bereaksi dengan air, menghasilkan perubahan pH larutan. Proses ini penting untuk memahami sifat asam-basa larutan garam dan perilaku ion dalam sistem akuatik. Pemahaman tentang hidrolisis ion sangat krusial dalam berbagai bidang, mulai dari kimia analitik hingga biokimia dan ilmu lingkungan.
Konsep Hidrolisis Ion dalam Reaksi Asam-Basa
Hidrolisis ion dapat dipahami sebagai reaksi asam-basa antara ion dan molekul air. Ion-ion yang berasal dari asam lemah atau basa lemah akan cenderung bereaksi dengan air, menghasilkan ion hidronium (H 3O +) atau ion hidroksida (OH –), sehingga mengubah pH larutan. Ion dari asam kuat dan basa kuat umumnya tidak mengalami hidrolisis secara signifikan karena konjugat asam-basa mereka sangat lemah.
Contoh Reaksi Hidrolisis Ion
Berikut beberapa contoh reaksi hidrolisis ion umum, yang menunjukkan bagaimana ion-ion tertentu berinteraksi dengan air:
- Hidrolisis Kation: Ion amonium (NH 4+), sebagai konjugat asam dari basa lemah amonia (NH 3), bereaksi dengan air menghasilkan ion hidronium dan amonia: NH 4+ + H 2O ⇌ H 3O + + NH 3. Larutan garam amonium akan bersifat asam.
- Hidrolisis Anion: Ion asetat (CH 3COO –), sebagai konjugat basa dari asam lemah asam asetat (CH 3COOH), bereaksi dengan air menghasilkan ion hidroksida dan asam asetat: CH 3COO – + H 2O ⇌ OH – + CH 3COOH. Larutan garam asetat akan bersifat basa.
Faktor-faktor yang Mempengaruhi Tingkat Hidrolisis Ion
Beberapa faktor mempengaruhi tingkat hidrolisis ion, antara lain:
- Kekuatan asam/basa konjugat: Semakin lemah asam atau basa konjugat, semakin besar tingkat hidrolisisnya.
- Konsentrasi ion: Konsentrasi ion yang lebih tinggi akan meningkatkan tingkat hidrolisis.
- Suhu: Suhu yang lebih tinggi umumnya meningkatkan laju reaksi hidrolisis.
Perbandingan Sifat Asam-Basa Beberapa Ion Umum
Tabel berikut membandingkan sifat asam-basa beberapa ion umum dan reaksi hidrolisisnya:
| Nama Ion | Rumus Kimia | Sifat | Reaksi Hidrolisis |
|---|---|---|---|
| Amonium | NH4+ | Asam | NH4+ + H2O ⇌ H3O+ + NH3 |
| Asetat | CH3COO– | Basa | CH3COO– + H2O ⇌ OH– + CH3COOH |
| Klorida | Cl– | Netral | Tidak mengalami hidrolisis signifikan |
Mekanisme Hidrolisis Ion, Ion berikut mengalami hidrolisis dalam air kecuali
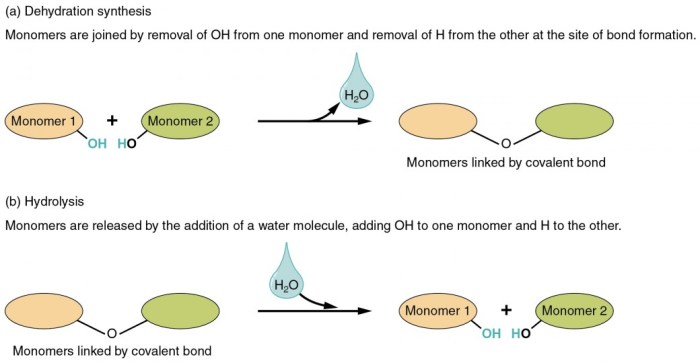
Mekanisme hidrolisis melibatkan interaksi antara ion dengan molekul air. Misalnya, pada hidrolisis ion amonium, atom hidrogen dari ion amonium ditransfer ke molekul air, membentuk ion hidronium dan amonia. Ikatan kovalen polar dalam molekul air memungkinkan transfer proton ini. Ilustrasi molekul air (dengan ikatan polarnya yang ditunjukkan dengan δ+ dan δ-) berinteraksi dengan ion amonium, menunjukkan bagaimana proton berpindah dari amonium ke molekul air, membentuk ion hidronium dan amonia.
Proses yang serupa terjadi pada hidrolisis anion, di mana ion hidroksida terbentuk melalui interaksi antara anion dan molekul air.
Ion yang Tidak Mengalami Hidrolisis
Hidrolisis merupakan reaksi antara ion dengan air, menghasilkan perubahan pH larutan. Namun, tidak semua ion mengalami hidrolisis. Beberapa ion bersifat netral dalam air dan tidak mengganggu kesetimbangan ion H + dan OH –. Pemahaman tentang ion-ion ini penting untuk prediksi sifat larutan dan perhitungan kesetimbangan kimia.
Ion yang tidak mengalami hidrolisis umumnya berasal dari asam kuat dan basa kuat. Hal ini karena asam dan basa kuat terionisasi sempurna dalam air, sehingga ion-ion yang dihasilkan tidak memiliki kecenderungan untuk bereaksi kembali dengan air membentuk asam atau basa lemah.
Ion-ion yang Tidak Mengalami Hidrolisis
Beberapa contoh ion yang termasuk dalam kategori ini antara lain ion natrium (Na +), kalium (K +), klorida (Cl –), nitrat (NO 3–), dan sulfat (SO 42-). Ion-ion ini berasal dari asam kuat (HCl, HNO 3, H 2SO 4) dan basa kuat (NaOH, KOH).
Alasan Ketidakmampuan Ion untuk Mengalami Hidrolisis
Ketidakmampuan ion-ion tersebut untuk mengalami hidrolisis terletak pada kekuatan asam dan basa induknya. Asam dan basa kuat terionisasi sempurna dalam air, sehingga ion-ion konjugatnya (ion yang dihasilkan setelah ionisasi) sangat lemah dan tidak cukup kuat untuk bereaksi dengan air. Dengan kata lain, ion-ion ini tidak memiliki afinitas yang signifikan terhadap proton (H +) atau hidroksida (OH –) dalam larutan.
Contoh Reaksi yang Menunjukkan Ketidakmampuan Ion untuk Bereaksi dengan Air
Sebagai contoh, perhatikan ion natrium (Na +). Ketika NaCl dilarutkan dalam air, ia terdisosiasi sempurna menjadi Na + dan Cl –. Tidak ada reaksi lebih lanjut antara Na + dan air karena Na + merupakan ion konjugat dari basa kuat NaOH yang sangat lemah. Reaksi yang terjadi hanya disosiasi:
NaCl(s) → Na+(aq) + Cl –(aq)
Hal serupa terjadi pada ion klorida (Cl –), yang merupakan ion konjugat dari asam kuat HCl. Cl – tidak bereaksi dengan air karena HCl merupakan asam kuat yang terionisasi sempurna.
Perbandingan Ion yang Mengalami dan Tidak Mengalami Hidrolisis
| Sifat | Ion yang Mengalami Hidrolisis | Ion yang Tidak Mengalami Hidrolisis |
|---|---|---|
| Asal | Asam lemah atau basa lemah | Asam kuat atau basa kuat |
| Derajat Ionisasi | Tidak sempurna | Sempurna |
| Pengaruh terhadap pH | Mengubah pH larutan | Tidak mengubah pH larutan (atau perubahannya sangat kecil dan dapat diabaikan) |
| Contoh | CH3COO–, NH4+ | Na+, K+, Cl–, NO3– |
Karakteristik Umum Ion yang Tidak Mengalami Hidrolisis
Ion yang tidak mengalami hidrolisis umumnya berasal dari asam kuat dan basa kuat, terionisasi sempurna dalam air, dan ion konjugatnya sangat lemah sehingga tidak bereaksi signifikan dengan air, sehingga tidak berpengaruh signifikan terhadap pH larutan.